آزمون تشخیص اختصاصیE. Coli
اشریشیا کلی (به اختصار E. coli) یک گیاه مشترک (فلور طبیعی) در روده انسان و حیوانات خونگرم است. بیشتر سویه های E.coli بی ضرر هستند، حتی برخی از آنها با تولید ویتامینK در روده برای میزبان مفید هستند. با این حال، برخی از سویه ها می توانند باعث بیماری های شدید ناشی از غذا شوند.
نشان داده شد که یک تراشه نانوبیوسنسور با استفاده از طیفسنجی رامان (SERS) تقویتشده سطحی روی لایههای نازک نانومجسمهسازی شده (nSTFs) نقره، باکتری اشریشیا کلی (E. coli) را تا سطح غلظت یک باکتری شناسایی میکند. این حسگر از nSTFهای پلاسمونیک بسیار پیشرفته نقره بر روی یک پلت فرم سیلیکونی برای تقویت باندهای رامان همانطور که با مولکول های 4-آمینوتیوفنول جذب شده بررسی می شود، استفاده می کند.
برای کسب اطلاعات بیشتر و دریافت خدمات با ما تماس بگیرید.
باکتریوفاژهای T-4 بر روی سطح فوق الذکر تراشه برای جذب خاص باکتری هدفE. coli بی حرکت شدند. برای نشان دادن اینکه هیچ بیحرکتی غیراختصاصی قابل توجهی در سایر باکتریها رخ نمیدهد، از سه سویه باکتریایی مختلف، کروموباکتریوم ویولاسئوم، پاراکوکوس دنیتریفیکانس و سودوموناس آئروژینوزا استفاده شد. علاوه بر این، آزمایشهایی که بر روی یک سویه اضافی ازE. coli برای پرداختن به ویژگی و قابلیت استفاده مجدد حسگر انجام شد، نشان داد که حسگر برای سویههای مختلفE. coli عمل میکند و قابل استفاده مجدد است. میکروسکوپ زمان حل و فصل کنتراست فاز تراشه باکتریوفاژE. coli-T4 برای مطالعه تعامل آن با باکتری در طول زمان انجام شد. نتایج نشان داد که حسگر حاضر تشخیص سریع، دقیق و پایدارE. coli را با غلظتهای بسیار کم باکتری تا سطح یک باکتری در حجم 10 میکرولیتر از نمونه انجام میدهد.
سابقه و هدف: E. coli O157:H7 یکی از پاتوژن های روده ای است که می تواند باعث ایجاد ضایعات شدید در دستگاه گوارش شود. این باکتری ها می توانند سموم تولید کنند و عامل اصلی عفونت های بیمارستانی هستند. تشخیص آنها معمولاً با کشت روی سوربیتول مک کانکی آگار انجام می شود که آزمایشی زمان بر است. هدف از این مطالعه ایجاد روشی سریع و در عین حال دقیق برای شناسایی این باکتری با استفاده از روش مبتنی برPCR بود.
مواد و روشها: ژنهای rfbE وstx2b جهت شناسایی کردن سویه اختصاصی E. coli O157:H7 انتخاب شده اند. سپس با طراحی پرایمرهای اختصاصی، تکثیر باPCR انجام شد. آگارSorbitol-MacConkey برای بررسی توانایی رشد کلنی های منتخب در طیPCR استفاده شد.
یافتهها: با توجه به ظاهر پیوندهای متعلق به ژنهای rfbE وstx2B روی ژل آگارز، توانایی پرایمرهای طراحیشده برای تشخیص ژن در نمونههایE.coli O157:H7 تأیید شد. برای ارزیابی قدرت رشد کلنی های انتخاب شده در طیPCR از محیط سوربیتول-مک کانکی آگار استفاده شد.
اشریشیا کلی: خواص و شناسایی
اشریشیا کلی (به اختصار E. coli) یک گیاه مشترک (فلور طبیعی) در روده انسان و حیوانات خونگرم است. بیشتر سویه های E.coli بی ضرر هستند، حتی برخی از آنها با تولید ویتامینK در روده برای میزبان مفید هستند. با این حال، برخی از سویه ها می توانند باعث بیماری های شدید ناشی از غذا شوند.
سویه های مختلف اشریشیا کلی و بیماری های ناشی از آنها
برخی از سویه های E. coli با به دست آوردن فاکتورهای حدت از طریق پلاسمیدها، ترانسپوزون ها، باکتریوفاژها و یا جزایر بیماری زایی به E. coli بیماریزا تبدیل شده اند. باکتریE. coli روده ای بیماری زا ممکن است بر اساس مکانیسم ایجاد اسهال به چهار سویه طبقه بندی شود. آن ها هستند؛ انتروهموراژیک (EHEC)، یا وروتوکسیژنیک (VTEC)، انتروتوکسیژنیک (ETEC)، انتروپاتوژنیک (EPEC) و انتروتهاجمی (EIEC) یا انتروآگرگاتیو (EAEC).
سویه های مولد اگزوتوکسین از اشریشیا کلی می توانند اسهال آبکی (غیر خونی) و اسهال خونی بسته به اگزوتوکسینی که تولید می کنند ایجاد کنند. به عنوان مثال، سویه های انتروتوکسیژنیک اشریشیا کلی یکی از علل شایع اسهال آبکی (همچنین به عنوان اسهال مسافرتی شناخته می شود) در کشورهای در حال توسعه است.
بیماری های ناشی ازE.coli
عفونت های دستگاه ادراری (UTI): E.coli شایع ترین علت عفونت های مجاری ادراری هم در جامعه و هم عفونت های بیمارستانی است.E.coli باعث بیش از 75 درصد مواردUTI می شود.
E.coli دومین عامل مهم سپسیس گرم منفی میله است
عفونت پری ناتال با E.coli (قرار گرفتن نوزاد با E.coli کلونیزه شده در کانال زایمان مادر در هنگام زایمان طبیعی) علت اصلی مننژیت نوزادی است.
اشرشیاکلی انتروتوکسیژنیک (ETEC) مسئول اسهال مسافرتی (اسهال آبکی) است.
سویه های انتروهموراژیک E.coli (یعنی شیگا توکسین STx تولید کنندهE. coli) باعث اسهال خونی و سندرم اورمیک همولیتیک (HUS) می شود.
ویژگی هایE.coli
رنگ آمیزی گرم: اشریشیا کلی یک میله کوتاه یا باسیل مستقیم گرم منفی است
سلول های اشرشیاکلی میله های کوچکی به طول 1.0-2.0 میکرومتر با شعاع حدود 0.5 میکرومتر هستند.
- coli شایع ترین بی هوازی اختیاری در روده بزرگ و مدفوع می باشد.
زمان تولید شدن به عبارتی دوبرابر شدن اشریشیا کلی 20 دقیقه است.
E.coli تخمیر کننده لاکتوز است که کلنی های صورتی درMacConkey آگار ایجاد می کند (این ویژگیE.coli را از سالمونلا و شیگلا متمایز می کند - دو شایع ترین پاتوژن روده)
خاصیت آنتی ژنی: بیشتر از 1000 نوع آنتی ژنی اشرشیاکلی وجود دارد.
آ. آنتی ژن های دیواره سلولی O (بیش از 150 نوع)
ب آنتی ژن H- تاژک (بیش از 50 نوع)
ج آنتی ژن کپسولی (بیش از 90 نوع)
عوامل بیماریزاE.coli
پیلی: به چسبیدن ارگانیسم ها به سلول های ژژنوم و ایلئوم در صورت عفونت روده کمک می کند. اپیتلیوم دستگاه ادراری در صورت عفونت دستگاه ادراری.
کپسول: با فاگوسیتوز تداخل دارد و نقش اصلی را در عفونت های سیستمیک ایفا می کند.
اندوتوکسین (لیپوپلی ساکارید): مسئول چندین ویژگی سپسیس گرم منفی مانند تب، افت فشار خون و انعقاد داخل عروقی منتشر (DIC) است.
اگزوتوکسین ها به عنوان مثال انتروتوکسین روی سلول های ژژنوم و ایلئوم اثر می گذارد و باعث اسهال می شود. سایر اگزوتوکسین ها وروتوکسین، سم شیگا مانند و غیره هستند.
مقالات بیشتر:
بایو بردن
تشخیص اختصاصی میکروبها
تست آلودگی مایکوپلاسمایی
شیر و فرآورده های آن
ویژگی های تشخیصیE.coli
طرحی برای شناسایی سریع E. coli.
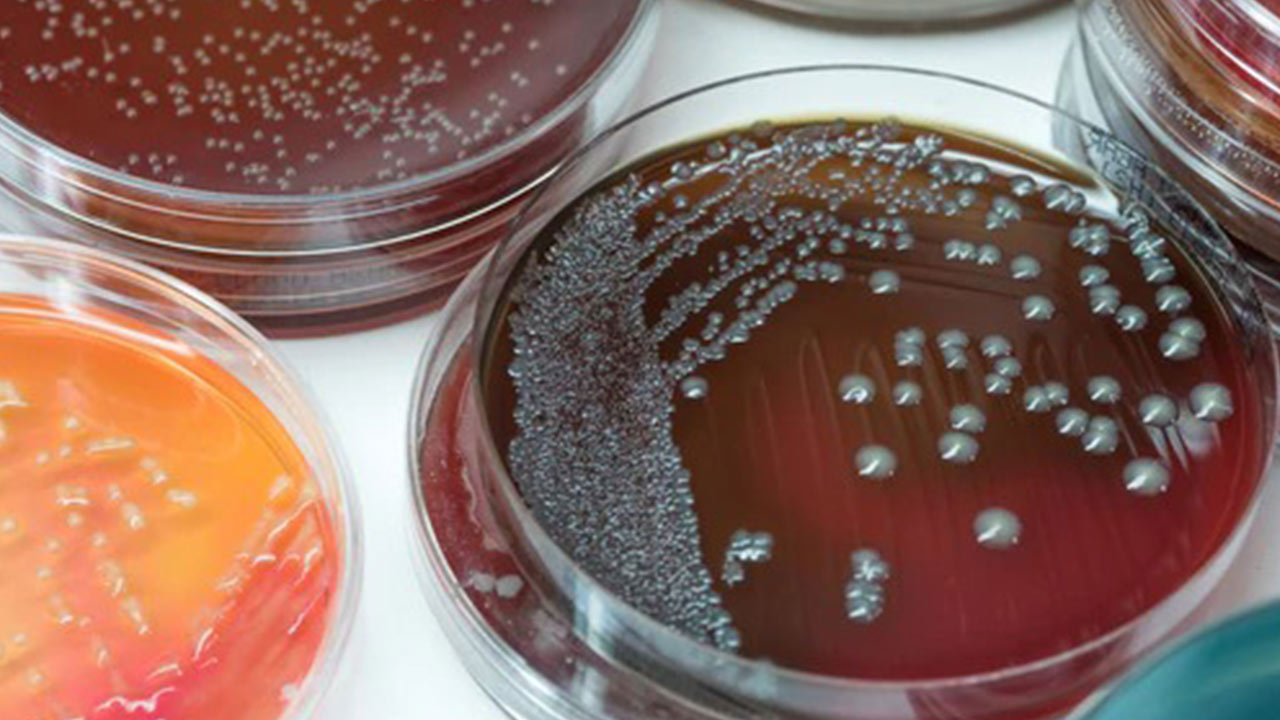
مورفولوژی کلنی: E.coli لاکتوز را تخمیر می کند و کلنی های صورتی درMacConkey Agar تولید می کند. کلنی های معمولی اشریشیا کلی در آگارMacConkey صورتی و براق ظاهر می شوند و پس از انکوباسیون یک شبه قطری بین 0.5 تا 1 میلی متر دارند. ظاهر کلنی از خاکستری تا سفید، شفاف تا مات، و به صورت محدب تا صاف روی صفحات خون آگار متفاوت است. با این حال، برخی ازE.coli متعلق به گروهAlkaligens-Dispar (A-D) ممکن است تخمیر غیر لاکتوز در Mac-Conkey آگار باشد. (E.coli O157: H7 سوربیتول را تخمیر نمی کند، که معیار مهمی است که آن را از سایر سویه هایE. coli متمایز می کند)
در آگار EMB، E. coli یک درخشش سبز مشخص ایجاد می کند.
آزمایشات بیوشیمیایی
ایندول مثبت: ایندول را از تریپتوفان تولید می کند
متحرک است
لیزین را دکربوکسیله می کند
از استات به عنوان تنها منبع کربن استفاده می کند
تست حساسیت ضد میکروبی
آزمایش حساسیت را با روش انتشار دیسک با استفاده از روش های استاندارد شرح داده شده در دستورالعمل ها انجام دهید. برای تشخیص E.coli مولدESBL، ایزوله غربال شده باید به چند دارو مقاوم باشد و حداقل به یکی از سفالوسپورین های نسل سوم مقاومت نشان دهد.
بتالاکتامازهای با طیف گسترده (ESBL) گروهی از بتالاکتامازها هستند که به سرعت در حال تکامل هستند که می توانند سفالوسپورین های نسل سوم و آزترئونام را هیدرولیز کنند اما توسط اسید کلاوولانیک مهار می شوند. افزایش مقاومت به سفالوسپورین های نسل سوم در میان باکتری E. coli عمدتاً به دلیل تولیدESBL است. این آنزیمهای واسطه پلاسمید عمدتاً از طریق جهش های نقطه ای کلاسیکTEM-1 وSHV-1 β-لاکتاماز تکامل یافته اند.
تست غربالگری برایE.coli تولید کنندهESBL
طبق دستورالعملهای CLSI، جدایه هایی که اندازه ناحیه بازداری ≤ 22 میلیمتر با سفتازیدیم (30 میکروگرم)، ≤ 25 میلیمتر با سفتریاکسون (30 میکروگرم)، و ≤ 27 میلیمتر با سفوتاکسیم (30 میکروگرم) را نشان می دهند ، بهعنوان تولیدک نندگان ESBL شناسایی م یشوند. در لیست نهایی تایید تولیدESBL قرار گرفت.
تست های تاییدی برایESBL
طبق دستورالعمل های CLSI، دو روش فنوتیپی می توانند تولیدکنندگان ESBL را تأیید کنند:
روش دیسک ترکیبی
این آزمایش مستلزم استفاده از دیسک آنتی بیوتیک سفالوسپورین نسل سوم به تنهایی و در ترکیب با اسید کلاوولانیک است. در این مطالعه، یک دیسک سفتازیدیم (30 میکروگرم) / سفوتاکسیم (30 میکروگرم) / سفپودوکسیم (30 میکروگرم) به تنهایی و یک دیسک از اسید کلاوولانیک مربوطه یا سفتازیدیم - اسید کلاوولانیک (30 میکروگرم / 10 میکروگرم) / سفوتاکسیم - اسید کلاوولانیک (30/ 10 میکروگرم/سفپودوکسیم – اسید کلاوولانیک (30/10 میکروگرم) استفاده می شود. هر دو دیسک با فاصله حداقل 25 میلی متر از هم ، مرکز به مرکز ، روی کشت چمن ایزوله آزمایشی روی صفحه مولر هینتون آگار (MHA) قرار می گیرند و یک شب در دمای 37 درجه سانتی گراد انکوبه می شوند. تفاوت در قطر منطقه با و بدون اسید کلاوولانیک اندازه گیری می شود.
تفسیر: افزایش ≥ 5 میلی متری در قطر ناحیه مهار در اطراف دیسک ترکیبی سفالوسپورین کلاوولانیک اسید در مقابل قطر ناحیه مهار در اطراف دیسک سفالوسپورین به تنهایی تولید ESBL را تایید می کند.
روش سینرژی دو دیسک
این آزمایش به دو دیسک از یک سفالوسپورین نسل سوم ، سفوتاکسیم ، سفتازیدیم یا سفپودوکسیم نیاز دارد. یک دیسک سفتازیدیم 30 میکروگرم و یک دیسک آموکسی سیلین + کلاوولانیک اسید 20 + 10 میکروگرم در فاصله 25 تا 30 میلی متری از هم ، مرکز به مرکز روی یک کشت چمن ایزوله آزمایش بر روی صفحه مولر هینتون آگار (MHA) قرار داده می شود.
تفسیر: تولید ESBL زمانی استنباط می شود که کلاوولانات ناحیه مهار را در اطراف دیسک سفتازیدیم به شکل برگ شبدری گسترش دهد.
مقالات بیشتر:
صحه گذاری بایوبردن
صحه گذاری استریلیتی
تست میکروبی اتاق تمیز
آزمون ماسک های پزشکی
اشرشیاکلی اروپاتوژنیک
سویه های اشرشیاکلی اروپاتوژنیک (UPEC) باعث 70 تا 90 درصد عفونت های مجاری ادراری اکتسابی از جامعه (UTIs) در حدود 150 میلیون نفر در سال و حدود 40 درصد از عفونت های بیمارستانی می شوند. ژن های حدت مختلف با عفونت های دستگاه ادراری ناشی از اشریشیا کلی مرتبط هستند.
اشرشیاکلی اروپاتوژن (UPEC)
سویه های اروپاتوژنیک اشرشیاکلی ، خواص ، محصولات یا ساختارهای باکتریایی متمایز (عوامل بیماری زای) را بیان می کنند که به آنها کمک می کند بر دفاع میزبان غلبه کنند و به مجاری ادراری کلونیزه یا حمله کنند.
در مقایسه با E.coli کامنسال،E.coli هایuropathogenic بهتر با مجرای ادرار سازگار هستند و نسبت بیشتری ازUTI ایجاد می کنند. هر چه یک سویه فاکتورهای حدت بیشتری را بیان کند، عفونت شدیدتری ایجاد می کند.
عوامل بیماری زایی که در پاتوژنز عفونت دستگاه ادراری (UTI) اهمیت دارند عبارتند از:
چسبنده ها (P fimbriae، برخی دیگر از چسبنده های مقاوم به مانوز، و fimbriae نوع 1): با اتصال به ساختارهای میزبان، از جاروب شدن توسط جریان طبیعی ادرار و دفع آن جلوگیری می کند. دلبستگی اولین گام ضروری در استعمار و سابقه ای برای عفونت تهاجمی در بسیاری از موقعیت ها است.
آنتی ژن K (پلی ساکارید کپسولی): آنها سلول را می پوشانند و در تشخیص آنتی ژن 0 اختلال ایجاد می کنند و از آن در برابر مکانیسم های دفاعی میزبان محافظت می کنند. کپسول دارای فعالیت ضد فاگوسیتیک و ضد مکمل است. میزان اختلال فاگوسیتوز با مقدار پلی ساکاریدها متناسب است.
مقاومت در برابر کشتن سرم: پلی ساکاریدهای کپسولی اسیدی و کپسول Kl با محافظت از باکتری ها در برابر فاگوسیتوز و احتمالاً از کشتن سرم، تا حدی با مسدود کردن فعال شدن مسیر مکمل جایگزین، به حدت کمک می کنند.
همولیزین: سم پروتئین سیتولیتیک که گلبول های قرمز تمام پستانداران را لیز می کند





